Newsletter
Was ist In-vitro-Fleisch?

In-vitro-Fleisch: Burger-Patties können auch im Labor gezüchtet werden, Bild: Pixabay, CCO
Fleisch aus dem Labor – das klingt für manche noch futuristisch. Burger-Patties und Steaks aus kultiviertem Fleisch sind aber bereits in der Realität angekommen und landen in einigen Ländern schon auf dem Tisch. Was In-vitro-Fleisch überhaupt ist, wie es hergestellt wird, was es kostet und wie es von Verbraucher:innen angenommen wird, beantwortet dieser Beitrag.
Kultiviertes Fleisch, Laborfleisch, Clean Meat (also „sauberes“ Fleisch) oder In-vitro-Fleisch – das sind alles Bezeichnungen für ein und dasselbe, nämlich ein Fleischersatzprodukt. Anstatt Tiere zu schlachten, wird dieses aus tierischen Zellen in vitro, also außerhalb eines lebenden Organismus in einer kontrollierten Laborumgebung, gezüchtet. Manche sehen In-vitro-Fleisch als Chance, der steigenden Fleischnachfrage mit einer nachhaltigeren und ethisch vertretbareren Alternative gerecht zu werden. Andere wiederum sehen es als Gefahr für die (Land-)Wirtschaft und Gesundheit.
Herstellung von In-vitro-Fleisch
Isolieren von Muskelstammzellen
Um Fleisch im Labor herstellen zu können, werden drei wichtige Komponenten benötigt: Zellen, Nährmedien und Bioreaktoren.
Die Basis für In-vitro-Fleisch sind Zellen, die durch eine Biopsie unter örtlicher Betäubung aus Tieren – wie beispielsweise Rindern, Hühnern oder Fischen – gewonnen werden [1-3]. Meist wird dabei Muskelgewebe entnommen, das dann zerkleinert und für die Zellkultur aufbereitet wird. Wichtig sind die darin enthaltenen Muskelstammzellen – seltene und sehr spezielle Zellen. Aus diesen gehen im Laufe eines Lebens die Muskelzellen eines Tieres hervor, und sie sind auch dafür zuständig, dass sich Muskeln nach einer Verletzung regenerieren. Unter Laborbedingungen können Muskelstammzellen neben Muskelzellen auch andere Zelltypen, wie beispielsweise Fettzellen, hervorbringen.
Kultivieren und vermehren von Muskelzellen
Zur Herstellung von Laborfleisch werden die Muskelstammzellen in Bioreaktoren vermehrt, in denen wachstumsbeeinflussende Parameter wie z.B. der pH-Wert oder die Temperatur konstant sind. Nährmedien liefern den Zellen wichtige Stoffe wie Aminosäuren, Vitamine, Proteine und Wachstumsfaktoren [4-6]. Eines dieser Medien ist das so genannte „Fetal Bovine Serum“ (FBS), welches alle nötigen Nährstoffe für das Zellwachstum der Muskelzellen in Kultur bereitstellt. Dieses Serum wird aus dem Blut ungeborener Kälber trächtiger Kühe gewonnen, wenn diese geschlachtet werden. Neben der Biopsie zur Zellgewinnung ist die Verwendung von FBS ein weiterer Grund, warum In-vitro-Fleisch erstens für Vegetarier:innen und Veganer:innen nicht geeignet und für viele prinzipiell ethisch nicht vertretbar ist [7]. Heute gibt es aber bereits Alternativen zu FBS für die In-vitro-Technologie (siehe auch unser Folgeartikel „In-vitro-Fleisch: Gamechanger für Umwelt und Ernährung?“).
Durch die richtigen Wachstumsbedingungen in Kultur entstehen aus Muskelstammzellen Muskelzellen, welche miteinander verschmelzen und Muskelfasern und -gewebe ausbilden. Durch die Zugabe bestimmter Hormone und Wachstumsfaktoren wird das Muskelwachstum angeregt [8], sodass aus nur ein paar Zellen in den Reaktoren mehr als eine Milliarde Muskelfasern entstehen können [9]. Und dies benötigt Zeit: Damit aus den Ursprungs-Zellen von der Biopsie in Kultur genügend Muskelfasern herangewachsen sind, um ein Burger-Patty oder Fleischlaberl daraus zu machen, vergehen mehrere Wochen.
„Bau“ der Laborfleischprodukte
Die Zellen in Kultur benötigen eine Matrix – also eine Oberfläche, an der sie sich „festhalten“ und dann wachsen können, sonst würden sie nämlich absterben. Die Lösung hierfür sind Mikroträger, an denen sich die Zellen festheften und zum Wachstum angeregt werden. Als Mikroträger dienen beispielsweise kleine Kugeln aus Kollagen oder aus Pektin. Bei Letzterem handelt es sich um einen Zucker, der in Zellwänden von Pflanzen zu finden ist und für den späteren Verzehr den Vorteil hat, dass er entweder essbar ist oder sich auflöst [10, 11].
Mit Mikroträgern kann man aber nur einfache Produkte wie etwa Burger-Patties herstellen. Um komplexere charakteristische Fleischstrukturen wie bei einem Steak nachzubauen, benötigt man zusätzlich ein schwammartiges Gerüst, das die grobe Struktur des Endprodukts vorgibt [4]. Um In-vitro-Steaks herzustellen, wird Muskelgewebe mittlerweile auch schon in 3D gedruckt [12].
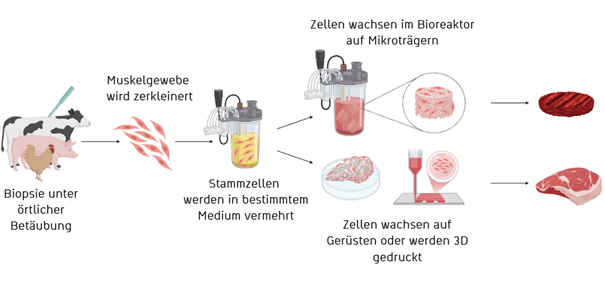
Der Prozess, Fleisch in vitro zu erzeugen, wird kontinuierlich optimiert. Um näher ans Original heranzukommen, kann man der Zellkultur oder dem 3D-Druck verschieden Zelltypen, wie beispielsweise Fettzellen oder Bindegewebszellen, beifügen, die dann im Endprodukt integriert sind.
Geschichte: Schon Churchill sah Potential von In-vitro-Fleisch
Die Menschheit isst Fleisch schon seit mehr als 2,6 Millionen Jahren. Mit dem Beginn der Tierzucht zwischen 8.000 und 5.400 v. Chr. wurde Fleisch zu einer leicht zugänglichen Nahrungsquelle. Durch die Industrialisierung im 19. und 20. Jahrhundert wurde Fleisch zunehmend günstiger und in größeren Mengen produziert. Bereits 1894 spekulierte der französische Chemiker Pierre Eugène Marcellin Berthelot, dass tierische Produkte bis zum Jahr 2000 in Fabriken synthetisch hergestellt werden könnten.
1912 gelang es dem französischen Chirurgen Alexis Carrel, embryonales Hühnerherzgewebe 34 Jahre lang in Zellkultur am Leben zu halten [13]. Dies war ein Schritt in die Richtung, in die auch der britische Politiker und Visionär Winston Churchill dachte. 1931 schrieb dieser in seinem Essay Fifty Years Hence, dass Fleisch in der Zukunft durch Zellkulturen erzeugt werden könnte, ohne Tiere zu schlachten.
Weitere Fortschritte ebneten in den darauffolgenden Jahrzehnten den Weg für die In-vitro-Fleisch-Technologie: In den 1950ern entwickelte sich die Zellkulturtechnologie, sodass Zellen isoliert und in Nährmedien kultiviert werden konnten. In den 1970er-Jahren kam dann das Tissue Engineering als wissenschaftliche Disziplin auf, die das Züchten von Zellen in 3D-Strukturen erlaubt.
Kurz vor der Jahrtausendwende gab es einen wichtigen Meilenstein in der Geschichte des Laborfleischs: 1999 erhielt der niederländischer Forscher und Geschäftsmann Willen von Eelen im Alter von 76 Jahren das erste Patent für die industrielle Produktion von kultiviertem Fleisch. Er gilt für seine Pionierarbeit bei der Herstellung und Entwicklung von Kulturfleisch als Gallionsfigur des Clean Meat. Sein Patent setzte die moderne Forschung zu In-vitro-Fleisch in Gang. 2002 gelang es NASA-Wissenschaftler:innen, Muskelgewebe aus einem Goldfisch zu kultivieren – ein Experiment, das zur Erforschung der Grundlagen für Zellkultur-Fleisch als Astronautennahrung diente [14].
Ein weiterer bahnbrechender Moment in der Geschichte von kultiviertem Fleisch erfolgte 2013: Mark Post, Forscher an der Universität Maastricht und Mitbegründer des niederländischen Unternehmens Mosa Meat, präsentierte öffentlich den weltweit ersten Burger mit einem In-vitro-Pattie. Hanni Rützler, österreichische Ernährungswissenschaftlerin und Foodtrendforscherin, war damals eine der nur zwei Testesserinnen. Der aus Stammzellen gezüchteten Burger aus Rindfleisch hatte enorme Produktionskosten, die je nach Quelle 250.000 bzw. 300.000 Euro betrugen. Post zeigte jedoch, dass die Herstellung von In-vitro-Fleisch technisch möglich war [15,16].
Seither hat sich einiges auf dem In-vitro-Markt getan: Im Jahr 2023 und somit rund zehn Jahre nach Posts Präsentation verzeichnete das Good Food Institute, die Denkfabrik der Laborfleisch-Branche, in sechs Ländern insgesamt 170 börsennotierte Unternehmen, die Fleisch oder Fisch aus Zellkultur weiterentwickeln und in naher Zukunft auf den Markt bringen wollen. Im selben Jahr wurden zehn neue Fabriken für In-vitro-Fleisch eröffnet. Neben diesen Unternehmen arbeiten noch etliche weitere an Lösungen, die den Produktionsprozess optimieren sollen [17].
Preise von In-vitro-Fleisch: Zu hoch und (noch) zu intransparent
Im Vergleich zu damals sind die Kosten für In-vitro-Fleisch heute moderat: Der Labor-Patty für einen Rindfleisch-Burger kostet aktuell etwa neun Euro. Und auch In-vitro-Hühnerfleisch ist mittlerweile leistbar geworden: Das israelische Unternehmen Believer Meats arbeitet seit Jahren an Fleisch aus Bioreaktoren und konnte den Preis für kultiviertes Hühnerfleisch auf rund 16 Euro pro Kilogramm senken [18,19]. Dennoch ist kultiviertes Fleisch noch immer teurer als konventionelles, vor allem aufgrund der hohen Kosten für Nährmedien, Bioreaktoren und Produktion. Um die Herstellungskosten von rund 48 Euro für ein einzelnes Chicken Nugget aus dem Labor zu senken, wurde das Unternehmen Eat Just aus Singapur erfinderisch: Es verkauft In-vitro-Hähnchennuggets, die mit Pflanzenproteinen „gestreckt“ und dadurch deutlich günstiger sind [20].
Das Start-Up SuperMeat hat es geschafft, die Produktionskosten für kultiviertes Hühnerfleisch auf 25 Euro pro Kilo zu senken, wenn die Produktion in 25.000-Liter-Bioreaktoren abläuft [21]. Zum Vergleich: Ein Kilogramm Hühnerfilet (von Masthühnern) kostete Anfang 2025 in österreichischen Supermärkten im Schnitt 8,80 Euro [22], wobei die Produktionskosten bei ungefähr 2,50 Euro lagen [23]. Dies entspricht somit nur ein Zehntel dessen, was das Unternehmen SuperMeat für einen Kilo In-vitro-Hähnchen aufwenden muss.
Ein wichtiger Treiber für die Senkung der Preise von In-vitro-Fleisch ist die Weiterentwicklung von Nährmedien ohne tierisches Serum. Denn mit rund 55 bis 95 Prozent der Produktionskosten fällt ein erheblicher Teil der Kosten für die Herstellung von In-vitro-Fleisch auf eben diese, insbesondere das Kälberserum. Der Preis für einen Liter Kälberserum liegt bei etwa 400 bis 800 Euro [18]. Hier gibt es allerdings frischen Wind: Das Unternehmen Believer Meats hat vor kurzem ein serumfreies Medium zu einem Preis von nur 60 Cent pro Liter vorgestellt, das zur Herstellung von Laborfleisch eingesetzt werden kann [24, 25].
Um den Preis von In-vitro-Fleischprodukten weiter zu senken, wird aktuell viel investiert – auch von Stellen, von denen man es nicht erwarten würde: So etwa beteiligte sich die PHW-Gruppe – das größte Unternehmen der Geflügelwirtschaft in Deutschland, zu dem die Geflügelmarke Wiesenhofer gehört – am Unternehmen Mosa Meat. Das US-amerikanische Unternehmen Memphis Meats wird unter anderem von Bill Gates und Richard Branson, dem Chef der Virgin-Group, dabei unterstützt, ihre Produkte weiter zu verbilligen. Kostete die Produktion eines halben Kilos Laborfleisch zu Beginn der In-vitro-Ära noch etwa 17.000 Euro, waren es vier Jahre später, im Mai 2017, schon „nur mehr“ rund 3.500 Euro. Das aktuelle Ziel ist es, ein halbes Kilo Laborfleisch um rund 5 Euro herstellen und so preislich mit konventionellem Fleisch mithalten zu können [26].
Auffallend ist, dass viele Unternehmen in der Laborfleischbranche ihre Preise aktuell geheim halten. Vermutlich halten sich viele aus Wettbewerbsgründen oder der noch nicht ganz klaren Marktbedingungen noch bedeckt.
Verbraucher:innenakzeptanz: Preis, Geschmack, Emotionen
Laborfleisch wird heute generell von Konsument:innen (noch) recht kritisch betrachtet. Dabei hängt deren Akzeptanz für In-vitro-Fleisch von dessen Geschmack und Preis ab, aber auch von ihrer Kultur und ihren Gewohnheiten.
Zweifel bestehen seitens der Verbraucher:innen teilweise bezüglich der Gesundheitsaspekte von Labornahrung und deren Sicherheit. In einer weltweiten Umfrage unter Personen, die noch kein In-vitro-Fleisch gegessen hatten, schätzte nur eine Minderheit dieses als schmackhaft und gesund ein. Die Mehrheit der Fleischesser:innen gab an, weiterhin „klassisches“ Fleisch zu bevorzugen [27].
Auch politische Einstellungen und Wissen über den Herstellungsprozess beeinflussen die Akzeptanz: So zeigte eine Studie aus den USA, dass Personen mit mehr Wissen über die Herstellung und einer linksorientierten politischen Einstellung eher dazu bereit waren, Laborfleisch zu probieren, als andere [28].
Natürlich spielt auch der Preis beim Kaufverhalten eine wichtige Rolle: Wäre Laborfleisch erheblich günstiger als herkömmliches Fleisch, würde auch die Bereitschaft steigen, dieses zu konsumieren [29,30]. Eine Preissenkung von In-vitro-Fleischprodukten könnte Konsument:innen eher dazu bringen, den Fleischkonsum zu reduzieren und auf Fleischalternativen, wie etwa In-vitro-Fleisch, umzusteigen [31]. In Schweden würde ein Drittel der befragten Konsument:innen bei günstigerem Preis auf Fleischersatz umsteigen. Allerdings lehnte fast die Hälfte der Befragten einen Laborfleisch-Burger ab, selbst wenn dieser kostenlos angeboten würde [32]. Auch eine weitere Studie kam zu dem Schluss, dass selbst sehr günstiges In-vitro-Fleisch nicht gekauft werden würde [33]. Besonders ältere Menschen und Personen ohne Hochschulbildung stehen Fleischersatzprodukten skeptisch gegenüber [32]. Österreicher:innen haben hier weniger Bedenken: So würden 42 Prozent von ihnen In-vitro-Fleisch zumindest einmal ausprobieren. Fast zwei Drittel wären dafür, es in Österreich zuzulassen, wenn die Lebensmittelsicherheit gewährleistet ist [34].
Soll Laborfleisch also wirklich einmal ein großer Player am Lebensmittelmarkt werden, gilt es hier neben der Weiterentwicklung der In-vitro-Technologie an sich auch noch allerhand an Aufklärungs- und Überzeugungsarbeit zu leisten. Hier spielen ethische und Umweltbedenken, der Wissensstand über die Thematik, persönliche Faktoren, wie Weltansichten, Glaube an einen persönlichen Vorteil oder Ernährungspräferenzen, sowie Emotionen eine Rolle [35]. Besonders die Angst vor neuen Lebensmitteln – die so genannte Lebensmittelneophobie – trägt dazu bei, dass Menschen ungern neue Lebensmittel ausprobieren [36]. Einige Wissenschaftler:innen sehen in der Angst vor neuen Lebensmitteltechnologien die stärkste Beeinflussung für die Akzeptanz von Fleischersatzprodukten [36-38].
Aber auch die Art und Weise, wie Informationen über In-vitro-Fleisch vermittelt werden, beeinflusst maßgeblich die Akzeptanz der Verbraucher:innen. So konnten Studien zeigen, dass die Wortwahl die Wahrnehmung von In-vitro-Fleisch stark beeinflusst. Der Begriff „kultiviertes Fleisch“ etwa führte zu positiveren Reaktionen als „im Labor gezüchtetes“ oder „künstliches“ Fleisch [39]. Die Emotionen von möglichen Konsument:innen sind auch nicht außer Acht zu lassen.
Resümee
Der weltweit erste Burger mit einem Patty, also einem Laibchen aus In-vitro-Fleisch, wurde 2013 der Öffentlichkeit präsentiert – mehr als 100 Jahre nachdem die Idee erstmals aufgekommen war, Fleisch synthetisch herzustellen. Seitdem wird daran getüftelt, Laborfleisch billiger, umweltfreundlicher und gesünder mit minimalem Tierleid zu produzieren. Der Herstellungsprozess von Laborfleisch beginnt aktuell mit der Entnahme von Muskelstammzellen aus Tieren. Die Zellen werden dann in Bioreaktoren unter kontrollierten Bedingungen mit Nährmedien versorgt und vermehrt.
Mikroträger und 3D-Druck ermöglichen heute die Herstellung von einfachen Fleischstrukturen wie Laibchen, aber auch die von komplexeren wie Steaks im Labor. Die Produktionskosten von In-vitro-Fleisch liegen immer noch über jenen von herkömmlichem Fleisch – einer der Punkte, weshalb die Akzeptanz der Verbraucher:innen noch gering ist. Ob es In-vitro-Fleischprodukte auf den Markt schaffen werden, hängt allerdings von mehreren Faktoren ab, wie etwa Gesundheitsbedenken, Kultur, Alter und Bildungsstand der Konsument:innen.
In-vitro-Fleisch hat jedenfalls das Potenzial, die Lebensmittelindustrie nachhaltig zu verändern. Doch bis dahin stehen noch Herausforderungen im Bereich der Kosten, Produktionskapazitäten und Verbraucherakzeptanz bevor. Die Weiterentwicklung der Technologie und eine gezielte Aufklärung könnten dazu beitragen, dass kultiviertes Fleisch langfristig eine echte Alternative zu konventionellem Fleisch wird.
Unser Beitrag „In-vitro Fleisch: Gamechanger für Umwelt und Ernährung?“ erörtert die möglichen Vorteile von Laborfleisch für unsere Gesundheit und die Umwelt.
cs, 24.03.2025
Quellenangaben
[1] Dodson M. V., Martin E. L., Brannon M. A., Mathiso, B. A. and McFarland, D. C.: Optimization of bovine satellite cell-derived myotube formation in vitro. Tissue & cell, 1987;19(2), 159–166.
[2] Yablonka-Reuveni Z., Quinn L.S. and Nameroff M.: Isolation and clonal analysis of satellite cells from chicken pectoralis muscle. Dev Biol. 1987;119(1):252-259.
[3] Powell R.L., Dodson M.V. and Cloud J.G.: Cultivation and differentiation of satellite cells from skeletal muscle of the rainbow trout Salmo gairdneri. J Exp Zool. 1989;250(3):333-338.
[4] Ben-Arye T., Levenberg S.: Tissue Engineering for Clean Meat Production. Front Sustain Food Syst. 2019;3(46).
[5] Asakura A., Komaki M. and Rudnicki M.: Muscle satellite cells are multipotential stem cells that exhibit myogenic, osteogenic, and adipogenic differentiation. Differentiation. 2001;68(4-5):245-253. doi:10.1046/j.1432-0436.2001.680412.x
[6] Brack A.S., Conboy I.M., Conboy M.J., Shen J. and Rando T.A.: A temporal switch from notch to Wnt signaling in muscle stem cells is necessary for normal adult myogenesis. Cell Stem Cell. 2008;2(1):50-59. doi:10.1016/j.stem.2007.10.006
[7] Bhat Z.F., Bhat H. and Pathak V.: Chapter 79- prospects for in vitro cultured meat a future harvest. Principles of Tissue Engineering. 4th ed. Boston, MA: Academic Press; 2014:1663-1683.
[8] Post M.J.: Cultured meat from stem cells: Challenges and prospects. Meat Sci. 2012;92(3):297-301.
[9] Allen R.E. and Boxhorn L.K.: Regulation of skeletal muscle satellite cell proliferation and differentiation by transforming growth factor-beta, insulin-like growth factor I, and fibroblast growth factor. J Cell Physiol. 1989;138(2):311-315.
[10] Bodiou V., Moutsatsou P. and Post M.J.: Microcarriers for Upscaling Cultured Meat Production. Front Nutr. 2020;7:10
[11] Modern Meadow Inc.: Edible and animal-product free microcarriers for engineered meat. WO 2015/038988 A1, 12.09.2014. Zuletzt aufgerufen am 27.09.2020.
[12] Derakhshanfar S., Mbeleck R., Xu K., Zhang X., Zhong W. and Xing M.: 3D bioprinting for biomedical devices and tissue engineering: A review of recent trends and advances. Bioact Mater. 2018;3(2):144-156. doi:10.1016/j.bioactmat.2017.11.008
[13]Benjaminson M.A., Gilchriest J.A. and Lorenz M.: In vitro edible muscle protein production system (MPPS): Stage 1, fish. Acta Astronaut. 2002;51:879-889. doi:10.1016/S0094-5765(02)00033-4
[14] Balasubramanian B., Liu W., Pushparaj K. and Park S.: The Epic of In Vitro Meat Production-A Fiction into Reality. Foods (Basel). 2021;10(6):1395. doi:10.3390/foods10061395
[15] Kumar P., Sharma N., Sharma S., Mehta N., Verma A.K., Chemmalar S. and Sazili A.Q.: In-vitro meat: a promising solution for sustainability of meat sector. J Anim Sci Technol. 2021 Jul;63(4):693-724. doi: 10.5187/jast.2021.e85. Epub 2021 Jul 31. PMID: 34447949; PMCID: PMC8367411.
[16] Kirsch M., Morales-Dalmau J. and Lavrentieva A.: Cultivated meat manufacturing: Technology, trends, and challenges. Eng Life Sci. 2023;23(12):e2300227. doi:10.1002/elsc.202300227
[17] Webartikel “Fleisch aus Zellkultur kommt auf den Markt: Ohne High-Biotech geht es nicht”, abgerufen am 10.03.2025
[18] Bandoim M.(2022) „Making Meat Affordable: Progress Since The $330,000 Lab-Grown Burger“ in: Forbes, abgerufen am 10.03.2025
[19] Webartikel „Future Meat: Israelisches Food-Unternehmen senkt Preis für Laborfleisch enorm“, abgerufen am 10.03.2025
[20] Webartikel “Laborfleisch, In-vitro-Fleisch, Clean Meat – Fleisch der Zukunft?”, abgerufen am 13.03.2025
[21] Webartikel „SuperMeat offers ‘glimpse into a future where cultivated meat can be produced at scale’ for $11.79/lb“, abgerufen am 10.03.2025
[22] Agar Markt Austria Preisbericht Februar 2025, abgerufen am 10.03.2025
[23] Agar Markt Austria Preisbericht September 2024, abgerufen am 10.03.2025
[24] Quek J. P., Gaffoor A. A., Tan Y. X., Tan T. R. M., Chua Y. F., Leong D. S. Z., Ali A. S. and Ng S. K.: Exploring cost reduction strategies for serum-free media development. npj Sci Food. 2024;8:107. doi:10.1038/s41538-024-00229-6.
[25] Pasitka L., Wissotsky G., Ayyash M., Yarza N., Rosoff G., Kaminker R. and Nahmias Y.: Empirical economic analysis shows cost-effective continuous manufacturing of cultivated chicken using animal-free medium. Nat Food. 2024 Aug;5(8):693-702. doi: 10.1038/s43016-024-01022-w. Epub 2024 Aug 21. PMID: 39179871.
[26] Forbes Artikel „Meat the Future: Foodamentalisten - Forbes“, abgerufen am 10.03.2025
[27] Hocquette A., Lambert C., Sinquin C., Peterolff L., Zoé W., Bonny S. P. F., Lebert A. and Hocquette J.-F.: Educated consumers don't believe artificial meat is the solution to the problems with the meat industry. J Integr Agric. 2015;14(2). doi:10.1016/S2095-3119(14)60886-8.
[28] Bryant C., Szejda K., Parekh N., Desphande V. and Tse B.: A Survey of Consumer Perceptions of Plant Based and Clean Meat in the USA, India, and China. Front Sustain Food Syst. 27. Februar 2019;3.
[29] Grasso A.C., Hung Y., Olthof M.R., Verbeke W. and Brouwer I.A.: Older consumers' readiness to accept alternative, more sustainable protein sources in the European Union. Nutrients. 2019;11(8):1.
[30] Barrena R. and Sánchez M.: Neophobia, personal consumer values and novel food acceptance. Food Qual Prefer. 2013;27(1):72-84.
[31] Tucker C.A.: The significance of sensory appeal for reduced meat consumption. Appetite. 2014;81:168-179. doi:10.1016/j.appet.2014.06.022
[32] Carlsson F., Kataria M. and Lampi E.: How much does it take? Willingness to switch to meat substitutes. Ecol Econ. 2022;193:107329. doi:10.1016/j.ecolecon.2021.107329.
[33] Van Loo E.J., Caputo V. and Lusk J.L.: Consumer preferences for farm-raised meat, lab-grown meat, and plant-based meat alternatives: Does information or brand matter? Food Policy. 2020;95:101931. https://www.sciencedirect.com/science/article/pii/S0306919220301354
[34] Studie der Veganen Gesellschaft: „Österreicher:innen sind kultiviertem Fleisch gegenüber aufgeschlossen“, abgerufen am 10.03.2025 https://www.vegan.at/inhalt/studie_kultiviertes_fleisch
[35] Pakseresht A., Ahmadi K.S. and Canavari M.: Review of factors affecting consumer acceptance of cultured meat. Appetite. 2022;170:105829. doi:10.1016/j.appet.2021.105829
[36] Asioli D., Bazzani C. and Nayga R.M.: Are consumers willing to pay for in-vitro meat? An investigation of naming effects. J Agric Econ. 2021. doi:10.1111/1477-9552.12467
[37] Gómez-Luciano C.A., de Aguiar L.K., Vriesekoop F. and Urbano B.: Consumers’ willingness to purchase three alternatives to meat proteins in the United Kingdom, Spain, Brazil and the Dominican Republic. Food Qual Prefer. 2019;78:103732.
[38] Hoefkens C., Verbeke W. and Van Camp J.: European consumers' perceived importance of qualifying and disqualifying nutrients in food choices. Food Qual Prefer. 2011;22(6):550-558.
[39] Hwang J., You J., Moon J. and Jeong J.: Factors affecting consumers' alternative meats buying intentions: Plant-based meat alternative and cultured meat. Sustainability. 2020;12(14):5662. https://www.mdpi.com/2071-1050/12/14/5662